今天匯總一下FDA上半年批准的新藥,共26款,Q1和Q2各13款,要顯著多於去年上半年的16款。其中輝瑞表現強勁,獲得三款新藥批准。
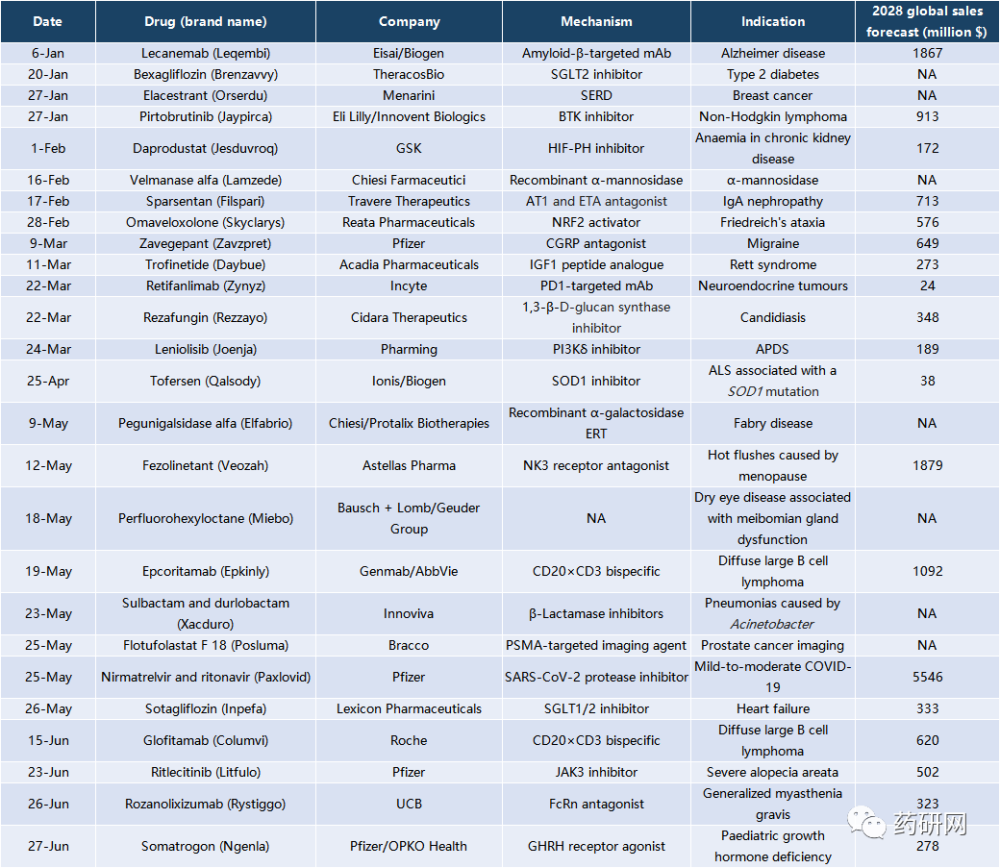
預計到2028年將有4款重磅炸彈:Paxlovid、Veozah、Lequmbi和Epkinly。
Paxlovid此前獲得緊急使用,在今年五月正式獲得了全面批准,但隨着疫情的減緩,人們對新冠藥需求的降低,其銷售額預計會從2022年的189億美元峰值降至2028年的55億美元。
Veozah是安斯泰來的NK3受體拮抗劑,原研公司爲Ogenda,該公司於2017年被安斯泰來收購。原定PDUFA目標日期是2月22日,後FDA延長至5月22日。Veozah是首款治療更年期潮熱的非激素療法,預計2028年銷額會達18.8億美元。
衛材/Biogen的Leqembi在1月獲加速批准上市,7月6日進一步獲得完全批准,成爲20年來首款獲完全批准的阿爾茲海默症新藥,定價2.65萬美元/年。預計2028年全球銷額會達到18.7億美元,但這是在加速批准的基礎上,完全批准後,美國醫療保險與醫療補助服務中心(CMS)會擴大覆蓋範圍,市場滲透率會進一步提高。
此外,上半年獲批的兩款雙抗均是CD3/CD20雙抗,分別是艾伯維/Genmab的Epkinly和羅氏的Columvi,適應症均是彌漫性大B細胞淋巴瘤(DLBCL)。
DLBCL是最常見的非霍奇金淋巴瘤類型。據估計,2022年美國該病患者達3.04萬例,而全球每年新增病例多達15萬例。
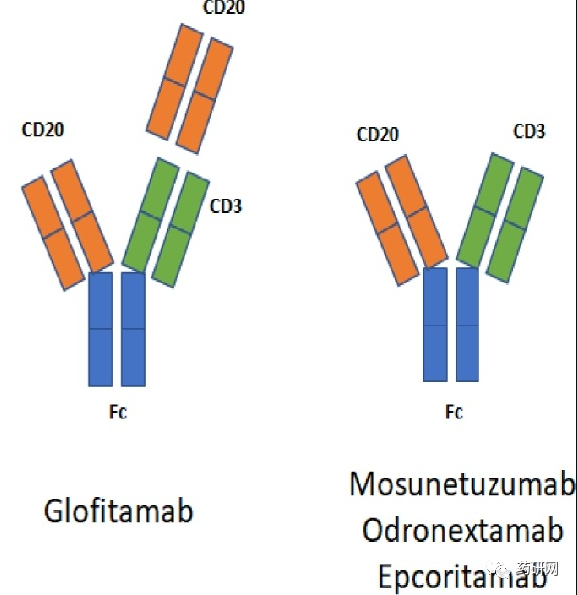
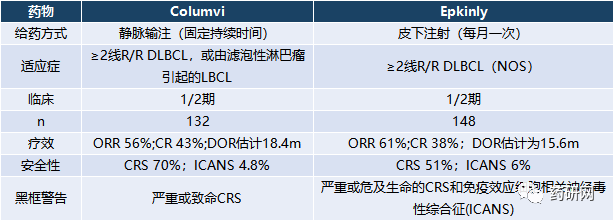
Epkinly的預期銷額要高於Columvi,主要是基於Epkinly的療效、給藥方式和安全性。
禮來的BTK抑制劑Jaypirca預計2028年銷額達到9.1億美元,這是FDA批准的首款也是唯一一款非共價BTK抑制劑,在此之前獲批的五款均爲共價抑制劑,獲批用於治療經過至少兩线系統治療(包括其他BTK抑制劑)的復發性或難治性套細胞淋巴瘤(MCL)成年患者。
雖已上市多款抑制劑,競爭激烈,但共價抑制劑會出現安全性或耐藥的問題,而Jaypirca可用於其他BTK抑制劑治療後進展的患者,同時安全性有所提高。
還有一些“第一”:
Reata公司的NRF2激動劑Skyclarys(omaveloxolone)是首個治療退行性神經肌肉疾病弗裏德賴希共濟失調症(FA)的產品,此前幾十年都未曾有藥物成功,而這款藥的獲批也是一波三折,從2020年被推遲後直到23年才成功獲批;
Acadia的IGF-1肽類似物Daubue是首個治療Rett綜合徵的藥物;
Menarini治療乳腺癌的藥物Orserdu是獲批的首個口服SERD,在此之前,阿斯利康的氟維司群(fulvestrant)是唯一獲批上市的 SERD 靶向藥,只能肌肉注射。
Chiesi的Lamzede是首個在美批准治療-甘露糖苷貯積症(AM)的非中樞神經系統表現的酶替代療法;
Pharming的PI3K抑制劑Joenja是首款用於APDS(一種原發性免疫缺陷病)治療的藥物,但該藥受衆相對較少,在美國僅發現了200名患者;
輝瑞的Zavzpret是首個治療偏頭痛的CGRP受體拮抗劑鼻腔噴霧,15分鐘即可發揮效果,此前8款CGRP/CGRPR類偏頭痛藥物均爲口服。
Cidara的棘白菌素類藥物Rezzayo十多年來首個批准用於念珠菌血症和侵襲性念珠菌病患者的新治療方案。
從這些第一中我們可以了解,在上半年獲批的藥物中,有多款藥打破了其治療領域“無藥可用,無藥可醫”的困局,讓衆多的罕見病患者有了希望。目前有很多罕見病,人們對其知之甚少,相關研究也不多,但隨着近幾年藥企對罕見病研發投入的加大,相信越來越多的罕見病人終有一天會被看見,會得以被治療。而有藥可醫的背後,也少不了研發團隊多年的堅持。
還值得一提的是,26款藥物中預計銷額最低的藥物是Incyte的PD1單抗 Zynyz,這是FDA批准的第五款PD1單抗,治療默克爾細胞癌(MCC),而Zynyz並不是第一款獲批MCC的PD1/PDL1抑制劑,較低的預估銷額主要是因爲激烈的競爭。
關注wechat藥研網
參考:
1.https://www.nature.com/articles/d41573-023-00065-1
2.https://www.nature.com/articles/d41573-023-00117-6
本文作者可以追加內容哦 !
標題:FDA 上半年批准的新藥匯總
地址:https://www.utechfun.com/post/237739.html
